Ошибка.
Попробуйте повторить позже
На -диаграмме отображена последовательность четырех процессов изменения состояния 2 моль идеального одноатомного
газа.
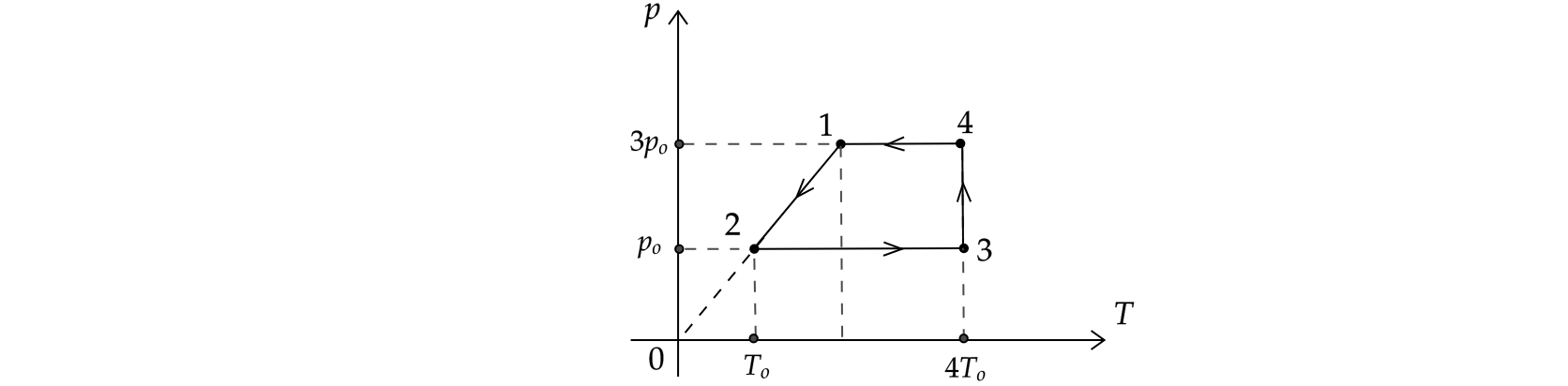
Из приведенного ниже списка выберите все правильные утверждения, характеризующих процессы на графике.
1) Газ за цикл совершает отрицательную работу.
2) Работа газа в процессе 1-2 максимальна по модулю.
3) В процессе 2-3 газ отдает положительное количество теплоты в окружающую среду.
4) Изменение внутренней энергии газа в процессе 1-2 в три раза больше, чем в состоянии 4-1.
5) В состоянии 3 объем газа максимален.
Для более удобной работы перестроим график из координат в координаты
:
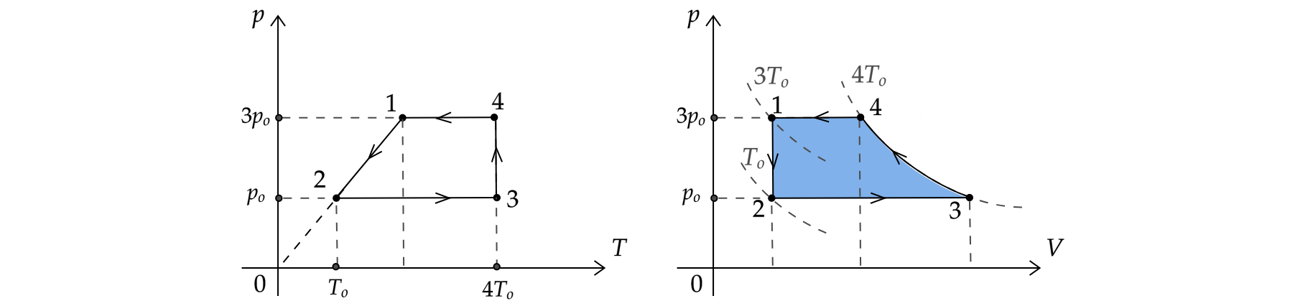
1)
Работа , совершенная газом за цикл, равна площади, заключенной внутри кривой 1-2-3-4-1. Так как объем газа уменьшается
(направление цикла против часовой стрелки), то работа цикла отрицательна.
2)
Работа газа зависит от изменения объема:
По графику (в -координатах это очевидно, в
-координатах можно исходить из того, что точки 1 и 2
лежат на одной изохоре) видно, что в процессе 1-2 объем газа остается неизменным. Следовательно, газ не совершает
работу.
3)
Процесс 2-3 — изобарный (т.к. ). Запишем первый закон термодинамики для изобарного процесса:
Работа газа зависит от изменения объёма газа:
По рисунку видно, что . Cледовательно, изменение объема положительно:
. Значит, газ совершил
положительную работу.
Изменение внутренней энергии газа зависит от температуры:
где — количество вещества газа,
— универсальная газовая постоянная.
Мысленно проведем две изотермы: и
. Так как изотерма
лежит ”выше” изотермы
, то
. Cледовательно,
изменение температуры положительно:
. Следовательно, и изменение внутренней энергии
также
положительно.
Так как изменение внутренней энергии газа и его работа положительны, то и количество теплоты также положительно,
поэтому газ не отдает теплоту, а получает ее.
4)
Найдем отношение изменений внутренних энергий и
.
Температуру можно найти из закона Гей-Люссака (т.к. процесс 1-2 изохорный):
Подставим это значение в предыдущую формулу:
5)
Исходя из графика в -координатах, очевидно, что утверждение верно.
На графике в -координатах можно провести изохоры и убедиться, что изохора
лежит ”ниже” всех остальных.
Следовательно, объем газа в состоянии 3 максимален.
Специальные программы

Программа
лояльности v2.0
Приглашай друзей в Школково и получай вознаграждение до 10%!

Крути рулетку
и выигрывай призы!
Крути рулетку и покупай курсы со скидкой, которая привязывается к вашему аккаунту.

Бесплатное обучение
в Школково
Для детей ДНР, ЛНР, Херсонской, Запорожской, Белгородской, Брянской областей, а также школьникам, находящимся в пунктах временного размещения Крыма обучение на платформе бесплатное.

Налоговые вычеты
Узнай, как получить налоговый вычет при оплате обучения в «Школково».

Специальное предложение
для учителей
Бесплатный доступ к любому курсу подготовки к ЕГЭ или олимпиадам от «Школково». Мы с вами делаем общее и важное дело, а потому для нас очень значимо быть чем-то полезными для учителей по всей России!

Вернём деньги за курс
за твою сотку на ЕГЭ
Сдать экзамен на сотку и получить обратно деньги за подготовку теперь вполне реально!




