Ошибка.
Попробуйте повторить позже
На pV-диаграмме показаны два процесса, проведённые с одним и тем же количеством газообразного аргона. Из приведённого ниже списка выберите все верные утверждения, характеризующие процессы на графике.
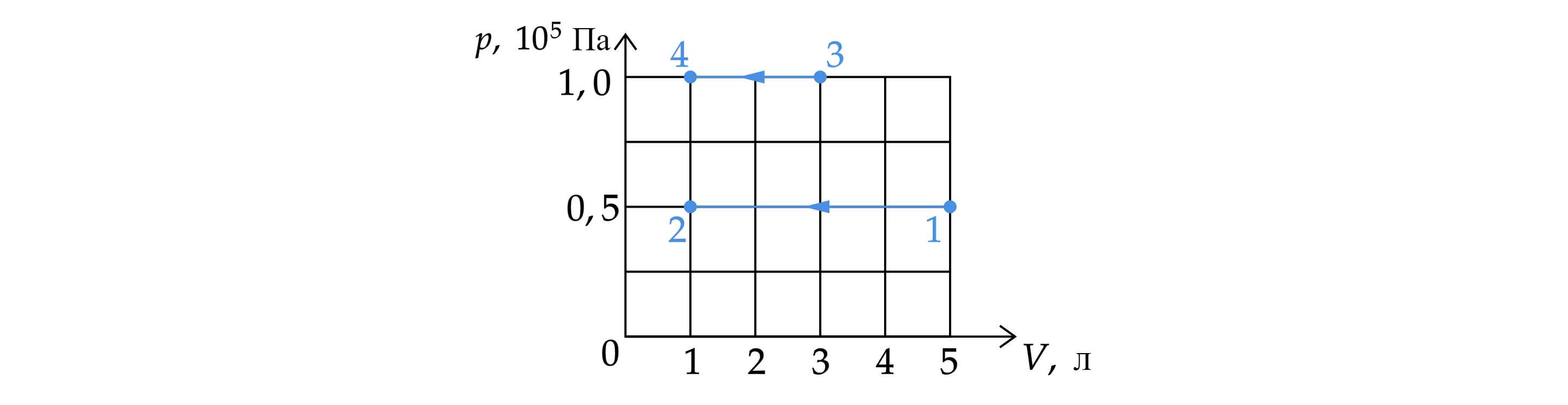
1) Работа, совершённая внешними силами над аргоном, в процессах 1–2 и 3–4 одинакова.
2) В процессе 3–4 абсолютная температура аргона изобарно уменьшилась в 5 раз.
3) В процессе 1–2 давление аргона в 2 раза больше, чем в процессе 3–4.
4) В процессе 1–2 аргон изобарно увеличил свой объём на 4 л.
5) В процессе 1–2 внутренняя энергия аргона уменьшилась в 5 раз.
1)
Работа над газом в изобарном процессе:
Тогда для первого и второго процесса:
То есть работа над газом в обоих процессах одинакова.
2)
Из закона Менделеева-Клапейрона для постоянного количества газа:
где – температура,
– количество вещества,
– универсальная газовая постоянная.
Так как давление постоянно, а объём газа уменьшается в 3 раза, то температура также уменьшается в 3 раза.
3)
Нет, по графику давление в 1-2 в раза меньше, чем в процессе 3-4.
4)
Нет, объём уменьшается на 4 л.
5)
Из закона Менделеева-Клапейрона для постоянного количества газа:
где – температура,
– количество вещества,
– универсальная газовая постоянная.
Так как давление постоянно, а объём газа уменьшается в 5 раза, то температура также уменьшается в 5 раза.
Внутренняя энергия равна
так как температура уменьшилась в 5 раз, то и внутренняя энергия уменьшается в 5 раз.
Ошибка.
Попробуйте повторить позже
В цилиндре под поршнем находится твердое вещество. Цилиндр поместили в раскаленную печь. На рисунке показан график
изменения температуры от вещества по мере поглощения им количества теплоты
.
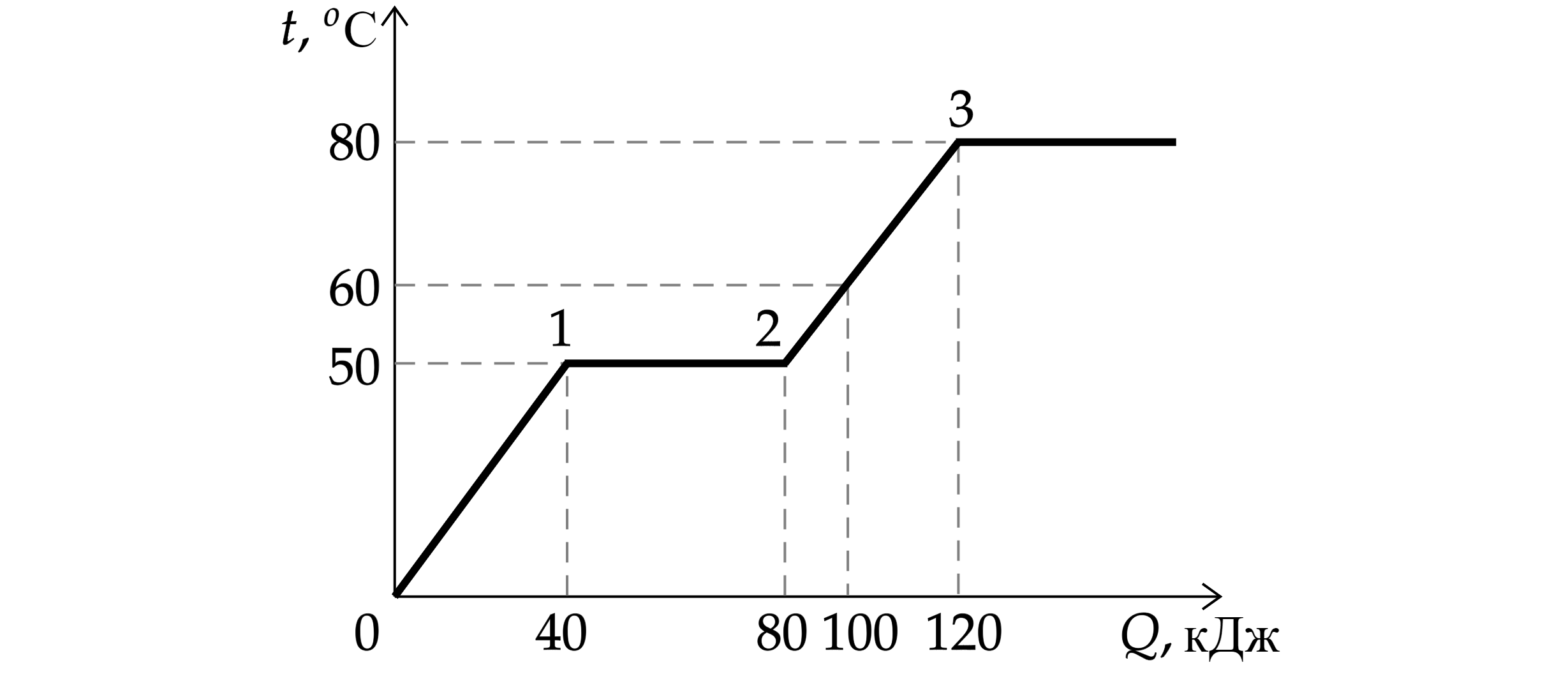
Выберите из предложенного перечня все верные утверждения. 1) Температура плавления вещества равна 50
.
2) Для того, чтобы полностью расплавить вещество, уже находящееся при температуре плавления, ему надо передать 80
кДж.
3) Когда тело получило 100 кДж оно полностью расплавилось.
4) Количество теплоты, которое необходимо затратить для нагревания тела от 60 до 80
равно 20 кДж.
5) Теплоемкость вещества в жидком состоянии меньше, чем в твердом.
1)
Температуру плавления показывает первая горизонтальная линия, то есть температура плавления .
2)
Нет, необходимо передать от точки 1 до точки 2, то есть 40 кДж.
3)
Да, уже начался нагрев жидкой фазы.
4)
Да, по графику это так.
5)
Для процесса нагрева справедлива формула:
где — удельная теплоемкость вещества,
— масса тела,
— изменение температуры.
То есть
При передачи 40 кДж в твердом состоянии тело нагревается на 50 , тогда как при передачи 40 кДж в жидком состоянии тело
нагрелось на 30
, то есть это неверно.
Ошибка.
Попробуйте повторить позже
1 моль одноатомного идеального газа совершает цикл 1-2-3-1, при котором давление газа изменяется с изменением плотности
газа так, как показано на рисунке. Значения плотности и давления в вершинах цикла представлены на графике. Выберите из
предложенного перечня все верные утверждения.
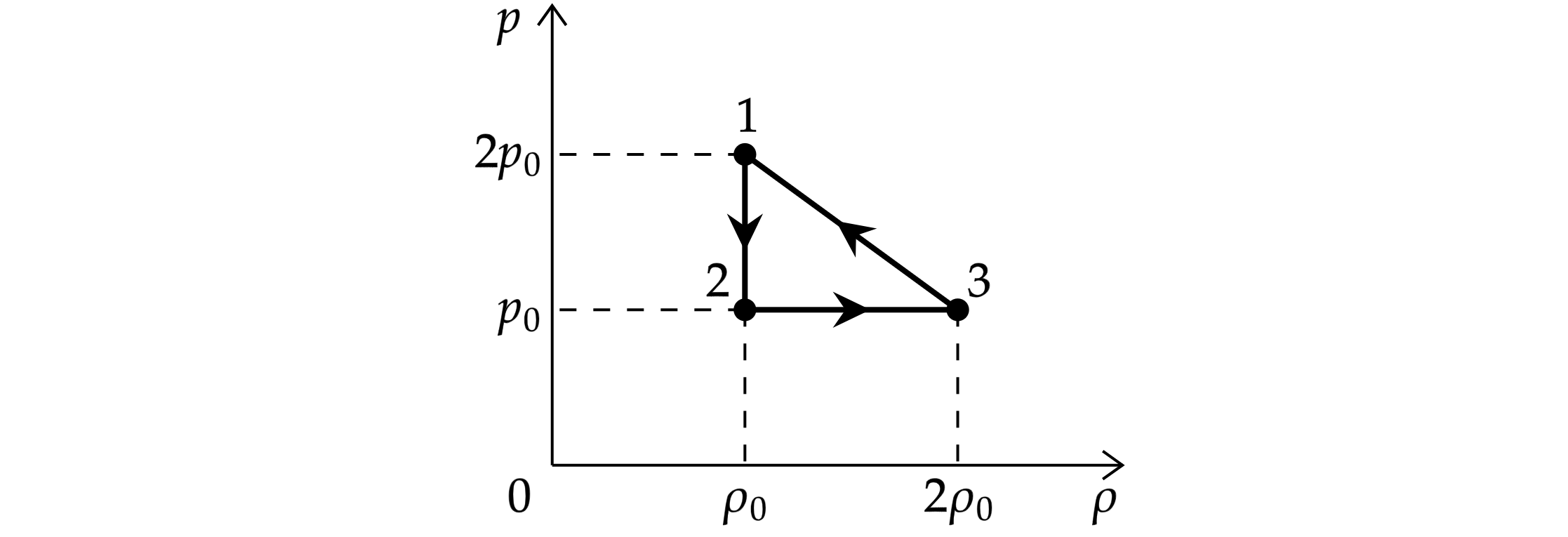
1) Работа газа в процессе 1-2 равна нулю.
2) В процессе 3-1 газ отдаёт положительное количество теплоты.
3) Температура газа в состоянии 3 минимальна.
4) Внутренняя энергия газа в процессе 2-3 увеличивается.
5) При переходе газа из 3 в 1 внутренняя энергия не меняется.
1)
Плотность газа найдем по формуле , где
– масса,
– объём газа.
Работа газа пропорциональна изменению объёма газа, так как в процессе 1-2 плотность постоянна, то изменение объёма рана нулю,
то и работа газа равна нулю.
2)
По первому началу термодинамики:
где – количество теплоты, полученное газом,
– изменение внутренней энергии,
– работа газа.
Внутренняя энергия равна:
где — количество вещества газа,
— универсальная газовая постоянная,
— абсолютная температура газа.
В процессе 3–1 плотность газа уменьшается, а объем увеличивается. Следовательно, работа газа на этом участке
положительна.
Запишем уравнение Менделеева – Клапейрона:
где — давление газа,
— объем, занимаемый газом.
Тогда
Для точек 3 и 1
То есть газ получает положительное количество теплоты.
3)
Из уравнения Клапейрона-Менделеева
где – молярная масса газа.
Отсюда
То есть температура в состоянии 3 минимальна.
4)
То есть внутренняя энергия уменьшается.
5)
См. пункт 2.
Ошибка.
Попробуйте повторить позже
Сосуд разделён на две равные по объёму части пористой неподвижной перегородкой. В начальный момент времени в левой части сосуда содержится 4 моль гелия, в правой – 20 г неона. Перегородка может пропускать молекулы гелия и является непроницаемой для молекул неона. Температура газов одинаковая и остаётся постоянной.
Выберите все верные утверждения, описывающих состояние газов после установления равновесия в системе.
1) Концентрация гелия в правой части сосуда в 2 раза больше, чем неона.
2) Отношение давления гелия в левой части сосуда к давлению газов в правой части сосуда равно 1,5.
3) В правой части сосуда общее число молекул газа меньше, чем в левой части.
4) Внутренняя энергия гелия и неона в сосуде одинакова.
5) В результате установления равновесия давление в правой части сосуда увеличилось в 3 раза.
Перегородка проницаема только для молекул гелия, поэтому в результате установления равновесия парциальное давление гелия в левой части будет равно парциальному давлению гелия в правой части. Давление газа можно вычислить по формуле:
Парциальные давления гелия в левой и правой части одинаковы, одинаковы температуры и объёмы частей, следовательно, одинаковы и количества вещества гелия в левой и правой частях сосуда, то есть в левой и правой части сосуда будет содержаться по 2 моля гелия.
Найдём связь концентрации и количества вещества:
То есть концентрации и количества вещества зависят прямо пропорционально друг от друга, также заметим, что чем больше количество вещества, тем больше и количество молекул.
Найдём количество вещества неона:
Используя полученное выше, рассмотрим данные в задании утверждения.
1)
Концентрация гелия в два раза больше концентрации неона в правой части сосуда.
2)
Отношение давлений:
где – количество вещества гелия в правой части, количество вещества гелия в левой части соответственно.
3)
Количество вещества газов в правой части сосуда больше количества вещества газа в левой части сосуда, следовательно, в правой части сосуда общее число молекул газа больше, чем в левой части сосуда.
4)
Внутренняя энергия одноатомного идеального газа может быть вычислена по формуле:
Температура газов одинакова. Количество вещества гелия больше количества вещества неона, следовательно, внутренняя энергия гелия больше внутренней энергии неона.
5)
Найдём отношение конечного давления в правой части сосуда к начальному давлению в правой части сосуда:
Ошибка.
Попробуйте повторить позже
В двух сосудах с одинаковыми объёмами находятся по 1 моль гелия и неона. В первом сосуде находится гелий при температуре
; во втором – неон при температуре 200 К.
Выберите все верные утверждения о параметрах состояния указанных газов.
1) Температура гелия выше, чем температура неона.
2) Среднеквадратичная скорость молекул гелия меньше, чем молекул неона.
3) Давление неона больше, чем давление гелия.
4) Средняя кинетическая энергия молекул неона в 2 раза меньше, чем молекул гелия.
5) Концентрация газов в сосудах одинакова.
1)
Температура гелия в Кельвинах равна К, что выше, чем температура неона
К
2)
Получим формулу зависимости средней квадратичной скорости от температуры. Cредняя кинетическая энергия поступательного
движения молекул газа
где – масса одной молекулы,
– молярная масса газов,
– постоянная Авогадро. Тогда
где – газовая постоянная. Запишем уравнение (1) для двух газов
, где для гелия кг/моль, для неона
кг/моль В итоге получаем
Среднеквадратичная скорость молекул гелия больше, чем молекул неона. 3)
Запишем уравнение Менделеева-Клапейрона:
где – давление газа,
– объём сосуда,
– количество вещества,
– температура газа.
Так как объёмы сосудов одинаковы, а температура неона меньше, чем температура гелия, то и давление неона меньше.
4)
Среднеквадратичная кинетическая энергия равна
так как температура гелия в 2 раза больше, то и средняя кинетическая энергия гелия в 2 раза больше.
5)
Найдём связь концентрации и количества вещества:
так как и количество вещества и объёмы сосудов одинаковы, то концентрации газов одинаковы.
Ошибка.
Попробуйте повторить позже
При переводе идеального газа из состояния 1 в состояние 2 давление газа пропорционально его плотности
(см. рисунок). Масса
газа в процессе остаётся постоянной.
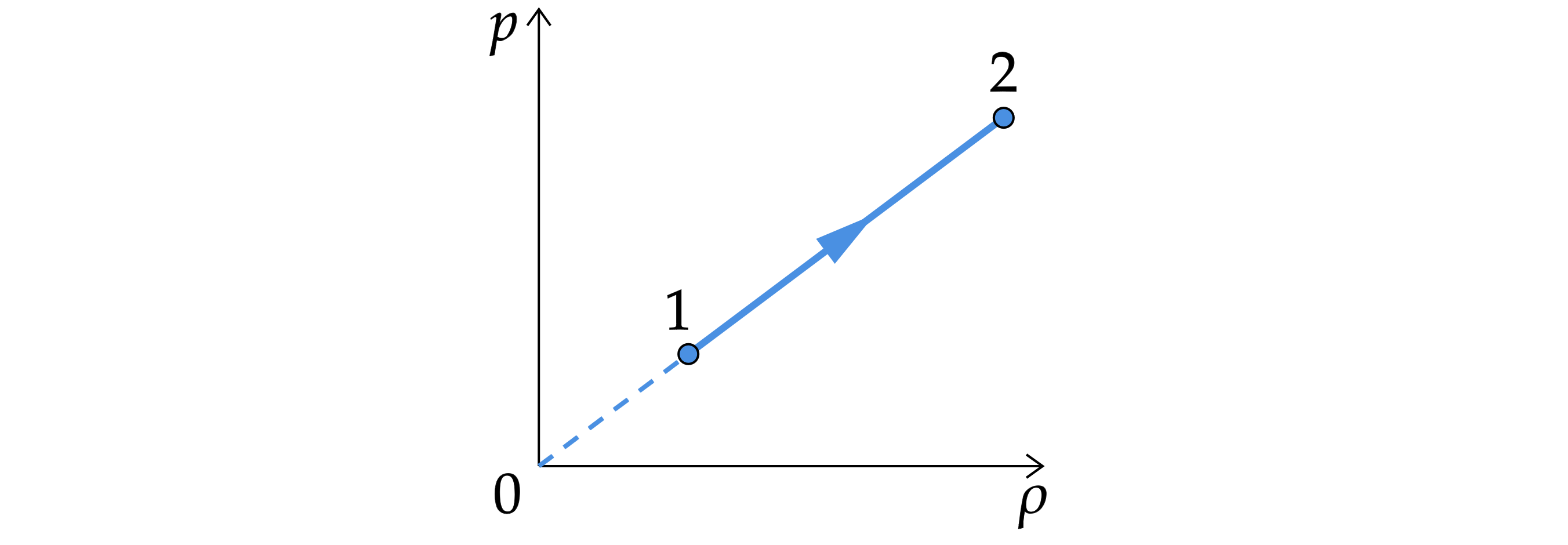
Из приведенного ниже списка выберите все верные утверждения, характеризующие процесс 1-2.
1) Абсолютная температура газа остается неизменной.
2) Концентрация молекул газа уменьшается.
3) Среднеквадратичная скорость теплового движения молекул газа увеличивается.
4) Средняя кинетическая энергия теплового движения молекул газа уменьшается.
5) Происходит изотермическое сжатие газа.
1)
По уравнению Клапейрона – Менделеева:
где – температура,
– молярная масса газа.
Так как и
имеют прямую пропорциональность
, где
– некоторый постоянный коэффициент,
то:
2)
Плотность газа равна
где – масса газа,
– его объём.
Так как масса газа не изменяется, то объём уменьшается.
Концентрация
где – количество молекул.
Количество молекул постоянно, а объём уменьшается, значит, концентрация увеличивается.
3)
Кинетическая энергия находится по формуле:
Так как температура постоянна, то и скорость постоянна.
4)
Кинетическая энергия
так как температура постоянна, то и кинетическая энергия постоянна.
5)
Да, температура постоянна, а объём уменьшается.
Ошибка.
Попробуйте повторить позже
В жестком герметичном сосуде объемом 1 при температуре 289 К длительное время находился влажный воздух и 5 г воды.
Сосуд медленно нагрели до температуры 298 К. Пользуясь таблицей плотности насыщенных паров воды, выберите все верные
утверждения о результатах этого опыта.
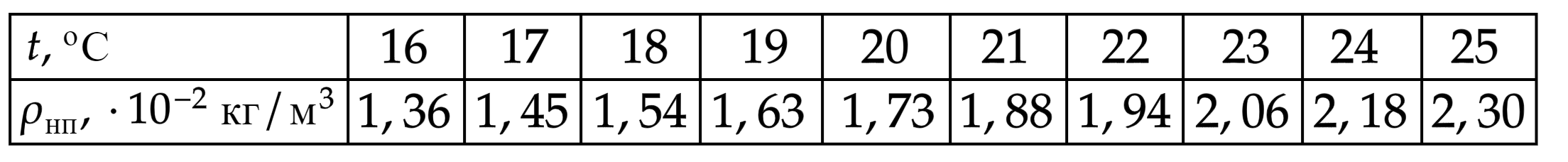
1) При температуре С влажность воздуха в сосуде была равна примерно 90,3%.
2) В течение всего опыта в сосуде находилась вода в жидком состоянии.
3) Так как объём сосуда не изменился, после испарения всей воды давление влажного воздуха увеличивалось пропорционально его абсолютной температуре.
4) В начальном состоянии при температуре 289 К пар в сосуде был ненасыщенный.
5) Парциальное давление сухого воздуха в сосуде монотонно возрастало.
1)
Если относительная влажность равна 90,3%, то вода полностью испарилась. Тогда масса пара при
равна
где – изначальная масса пара,
– изначальная масса воды,
– изначальная плотность водяных паров,
– объём
сосуда.
Значит, плотность пара
Относительная влажность равна
Тогда
2)
Нет, в вся вода испарилась.
3)
Запишем уравнение Менделеева-Клапейрона для водяного пара:
где – давление,
– объём сосуда,
– масса водяного пара,
– температура в Кельвинах.
Так как при полном испарении масса водяного пара не изменяется, то
То есть прямо пропорционально температуре.
4)
Нет, изначально в сосуде есть вода, значит, пар насыщенный.
5)
Да, давление сухого воздуха в сосуде описывается уравнением Менделеева-Клапейрона
То есть прямая пропорциональность.
Ошибка.
Попробуйте повторить позже
Медную кастрюлю наполнили на 3/4 водой, закрыли лёгкой крышкой и спустя несколько часов поставили на огонь. Воду в кастрюле довели до кипения и кипятили в течение некоторого времени. Атмосферное давление составляло 760 мм рт. ст. Выберите все верные утверждения, описывающие характеристики воды, водяного пара и кастрюли.
1) Относительная влажность воздуха под крышкой в процессе нагревания воды увеличивалась.
2) В ходе кипения воды средняя потенциальная энергия взаимодействия молекул воды, переходящих из жидкости в пар, увеличивается.
3) Давление водяных паров под крышкой в ходе процесса нагревания воды увеличивалось.
4) Температура медного дна кастрюли с водой при кипении немного меньше .
5) Плотность насыщенных водяных паров над поверхностью воды при нагревании до кипения оставалась постоянной.
1)
Так как после наполнения водой кастрюлю начали кипятить только через несколько часов, то первоначально относительная влажность воздуха в кастрюле была равна 100%. При этом так как в кастрюле при нагревании остается вода, то относительная влажность в кастрюле остаётся равной 100%, то есть не изменяется.
2)
Потенциальная энергия взаимодействия молекул при переходе из жидкости в пар увеличивается.
3)
Давление насыщенных паров в ходе увеличения температуры увеличивается. Давление водяных паров при 100% влажности равно давлению насыщенных паров, значит, давление водяных паров при нагреве увеличивается.
4)
Да, так как температура огня выше , при этом давление у дна кастрюли немного выше, чем атмосферное, так как у дна
кастрюли дополнительно давит столб жидкости в кастрюле, значит, температура закипания воды у дна чуть больше
,
следовательно, температура дна кастрюли чуть выше
.
5)
Плотность насыщенных водяных паров над поверхностью воды при нагревании до кипения возрастает.
Ошибка.
Попробуйте повторить позже
Объём сосуда, содержащего 1 моль неона, уменьшили вдвое и добавили в сосуд 1 моль аргона. Температура в сосуде поддерживается постоянной. Выберите из предложенного списка все утверждения, которые верно отражают результаты этого опыта.
1) Концентрация атомов неона в 2 раза меньше, чем у аргона.
2) Парциальное давление неона увеличилось в 2 раза.
3) Внутренняя энергия неона уменьшилась.
4) Плотность газа в сосуде увеличилась.
5) Давление в сосуде увеличилось в 4 раза.
1)
Концентрация:
где – количество молекул,
– объём сосуда.
Так как добавили 1 моль аргона, то и неона и аргона стало по 1 моль каждого, значит, их концентрации равны.
2)
Так как процесс изотермический, то по закону Бойля-Мариотта:
3)
При постоянстве массы газа его внутренняя энергия определяется только температурой. И, так как температура была постоянной, то
внутренняя энергия оставалась неизменной.
4)
Плотность газа равна:
где – масса газа.
Так как масса газа увеличилась (в газ добавили 1 моль аргона), а объём уменьшили, то плотность увеличилась.
5)
Давление газа можно найти из уравнения Менделеева-Клапейрона:
где – давление,
– количество вещества,
– температура.
Отсюда давление
так как количество вещества увеличилось в 2 раза, а объём уменьшился в 2 раза, то давление увеличилось в 4 раза.
Ошибка.
Попробуйте повторить позже
В сосуде под поршнем при комнатной температуре долгое время находятся вода и водяной пар. Масса воды равна массе пара. Объём сосуда медленно изотермически увеличивают в 3 раза.
Выберите все утверждения, которые верно отражают результаты этого опыта.
1) Плотность пара в начале и конце опыта одинакова.
2) Давление пара сначала было постоянным, а затем стало уменьшаться.
3) Концентрация пара в сосуде в начале опыта меньше, чем в конце опыта.
4) В конечном состоянии давление пара в сосуде в 3 раза меньше первоначального.
5) Масса пара в сосуде увеличивается в 2 раза.
1)
Так как вода и пар находятся под поршнем долгое время, то между ними устанавливается динамическое равновесие. При
увеличении объёма вода начинает испаряться до тех пор, пока полностью не испарится или пока увеличение объёма не прекратится.
Определим во сколько раз надо увеличить объём для полного испарения воды. Пусть масса пара и воды равны .
Запишем уравнение Менделеева-Клапейрона:
где – давление водяного пара,
– объём,
– количество вещества,
– молярная масса,
– температура.
При испарении пар остается насыщенным, значит, давление постоянно. Тогда запишем уравнение Менделеева-Клапейрона для начального состояния и состояния в котором полностью испарилась вода:
Так как по условию , то
То есть необходимо увеличить объём в 2 раза для полного испарения воды. После полного испарения воды масса пара не будет увеличиваться. Плотность можно найти по формуле:
В начальном состоянии
В конечном состоянии
То есть они не равны.
2)
Давление пара при испарении воды постоянно (так как пар остается насыщенным), затем оно подчиняется уравнению Менделеева-Клапейрона:
Так как при , масса пара становится постоянной, то при увеличении объёма давление пара начинает
уменьшаться.
3)
Концентрация пара:
где – количество молекул пара.
Так как при испарении воды количество молекул увеличивается в 2 раза, а объём увеличивается в 3 раза, то концентрация уменьшается.
4)
Нет, отношение давлений равно:
5)
Да, см. пункт 1.
Ошибка.
Попробуйте повторить позже
В цилиндрическом сосуде, закрытом подвижным поршнем, находится водяной пар. При постоянной температуре с паром провели
процесс ,
-диаграмма которого представлена на рисунке.
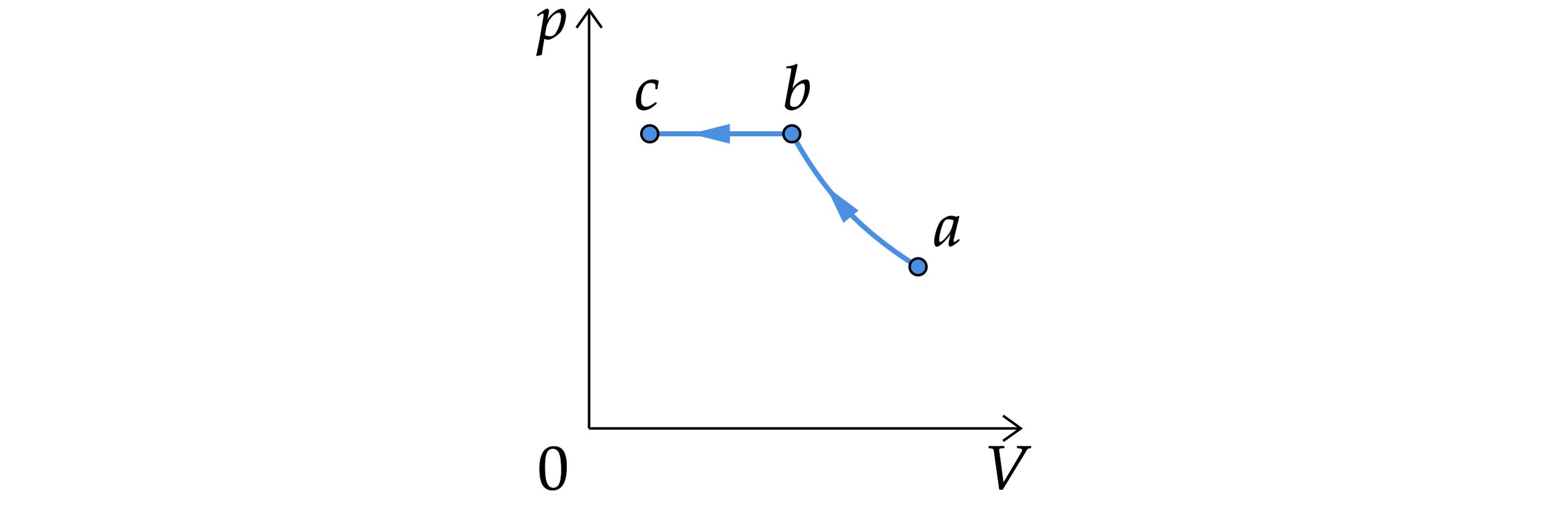
Из приведенного ниже списка выберите все верные утверждения относительно этого процесса.
1) На участке плотность пара увеличивается.
2) На участке к веществу в сосуде подводится положительное количество теплоты.
3) В точке водяной пар является насыщенным.
4) На участке внутренняя энергия пара уменьшается.
5) На участке к пару подводится положительное количество теплоты.
1) В процессе пар ненасыщенный, не происходит дополнительного испарения воды и масса пара постоянна. Плотность пара
равна:
так как уменьшается, то плотность увеличивается.
Утверждение 1 –
2) На участке происходит конденсация, при конденсации выделяется энергия, значит, пар отдает некоторое количество
теплоты.
Утверждение 2 –
3) Давление водяного пара описывается уравнением Менделеева-Клапейрона:
где – количество вещества,
– масса пара,
– молярная масса пара,
– температура.
Так как в процессе температура, молярная масса, универсальная газовая постоянная и давление постоянны, а объём
уменьшается, то
то есть количество водяного пара уменьшается за счет испарения воды и пар в является насыщенным.
Утверждение 3 –
4) Давление водяного пара описывается уравнением Менделеева-Клапейрона:
где – количество вещества,
– масса пара,
– молярная масса пара,
– температура.
Так как в процессе температура, молярная масса, универсальная газовая постоянная и давление постоянны, а объём
уменьшается, то
то есть количество водяного пара уменьшается за счет испарения воды. Так как количество пара уменьшается, то уменьшается и
внутренняя энергия пара.
Утверждение 4 –
5) На участке пар является ненасыщенным. Запишем первый закон термодинамики:
Объем уменьшается, значит, работа газа отрицательно. Внутренняя энергия не изменяется, так как температура пара по условию
постоянна.
Значит, отводят некоторое количество теплоты. Утверждение 5 –
Ошибка.
Попробуйте повторить позже
На рисунке показаны два процесса, проведённых с одним и тем же количеством газообразного неона ( – давление неона;
– его
объём).
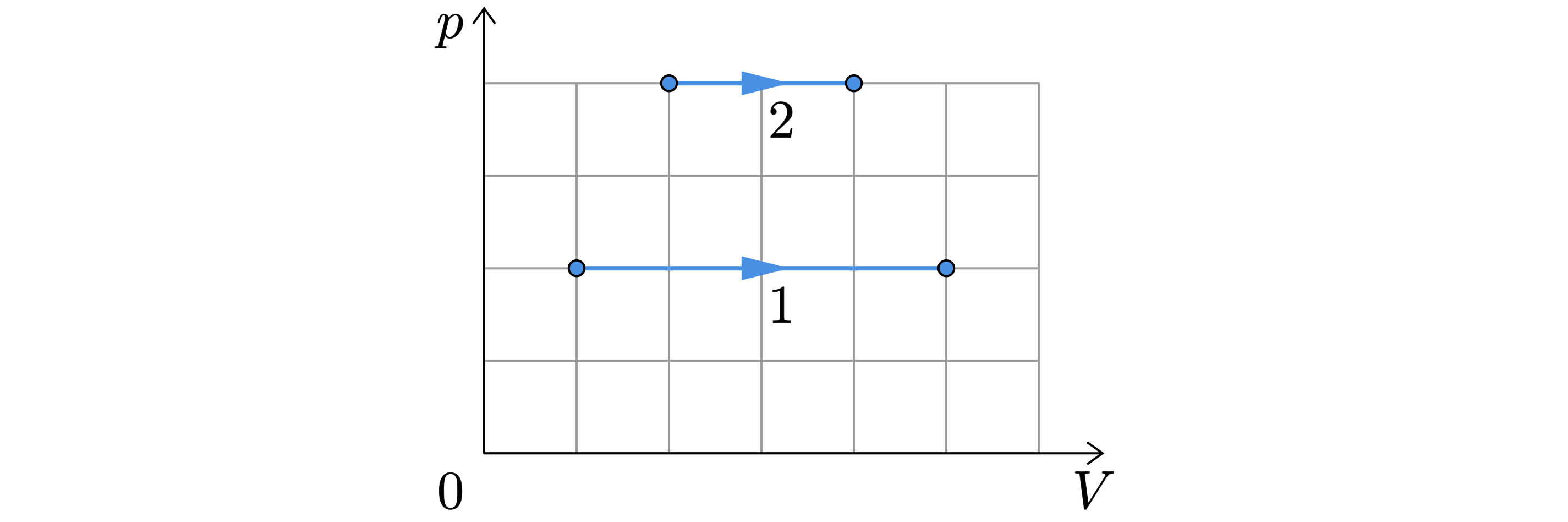
Из приведённого ниже списка выберите все верные утверждения, характеризующие процессы на рисунке.
1) В процессе 2 абсолютная температура неона изобарно увеличилась в 2 раза.
2) В процессе 1 плотность неона увеличилась в 5 раз.
3) В процессе 1 неон изобарно увеличил свой объём в 5 раз.
4) В процессе 2 концентрация молекул неона увеличилась в 2 раза.
5) Работа, совершенная неоном в процессе 1, больше, чем в процессе 2.
1)
Из закона Менделеева-Клапейрона для постоянного количества газа:
где – температура,
– количество вещества,
– универсальная газовая постоянная.
Так как давление равно, а объём газа увеличился в 2 раза, то температура также увеличилась в 2 раза.
2)
Плотность равна:
где – масса газа.
Так как объем увеличился в 5 раз, то плотность уменьшилась в 5 раз.
3)
Да, объём увеличился в 5 раз.
4)
Концентрация:
где – количество молекул.
То есть при увеличении объёма в 2 раза концентрация уменьшилась в 2 раза.
5)
Работа газа в изобарном процессе:
Тогда для первого и второго процесса:
То есть работа газа в обоих процессах одинакова.
Ошибка.
Попробуйте повторить позже
При переводе одноатомного идеального газа из состояния 1 в состояние 2 концентрация молекул пропорциональна давлению
(см. рисунок). Масса газа в процессе остаётся постоянной.
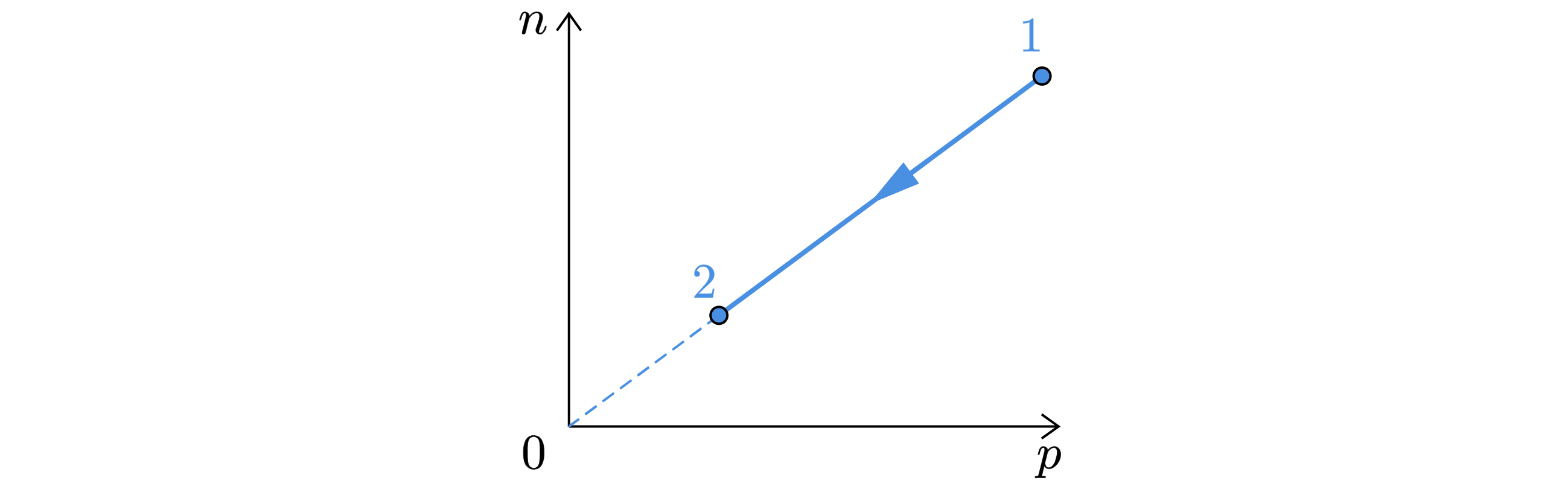
Из приведённого ниже списка выберите все правильные утверждения, характеризующих процесс 1-2.
1) Средняя кинетическая энергия теплового движения молекул газа остаётся неизменной.
2) Среднеквадратичная скорость теплового движения молекул газа увеличивается
3) Объём газа изотермически увеличивается.
4) Абсолютная температура газа уменьшается.
5) Плотность газа увеличивается.
1)
Запишем основное уравнение МКТ:
где — концентрация молекул,
— температура в Кельвинах,
— давление газа. Из графика видно, что
, значит,
процесс происходит при постоянной температуре (
) Среднеквадратичная скорость теплового движения молекул газа
равна:
2)
См. пункт 1.
3)
Концентрация в процессе уменьшается
где — количество молекул,
— объем, занимаемый молекулами. Концентрация уменьшается, при постоянном количестве
молекул, то есть объём изотермически увеличивается.
4)
Запишем основное уравнение МКТ:
где — концентрация молекул,
— температура в Кельвинах,
— давление газа. Из графика видно, что
, значит,
процесс происходит при постоянной температуре (
)
5)
Объем в этом процессе увеличивается, масса не изменяется, следовательно, плотность уменьшается.
Ошибка.
Попробуйте повторить позже
Идеальный газ переводят из состояния 1 в состояние 3 так, как показано на графике зависимости давления газа от объёма
.
Масса газа в процессе не изменяется. Из приведенного ниже списка выберите все верные утверждения, характеризующие
отраженные на графике процессы.

Из приведённого ниже списка выберите все верные утверждения, характеризующие отражённые на графике процессы.
1) Концентрация молекул газа в процессе 2-3 оставалась постоянной.
2) В ходе процесса 1-2-3 средняя кинетическая энергия теплового движения молекул газа увеличивается в 3 раза.
3) В процессе 2-3 абсолютная температура газа изохорно увеличилась в 1,5 раза.
4) В процессе 1-2 абсолютная температура газа изобарно увеличилась в 4 раза.
5) Абсолютная температура газа минимальна в состоянии 3.
1)
Концентрация равна:
где – количество молекул газа,
– объём.
Так как масса газа одинакова, то постоянна, по графику
тоже постоянна, значит, концентрация постоянна.
2)
Средняя кинетическая энергия равна:
где – температура газа.
Процесс 1-2 — изобарное расширение (). Объем увеличился в 2 раза, то есть температура тоже увеличилась в 2 раза.
Процесс 2-3 — изохорное нагревание.
, следовательно,
Давление увеличивается в 1,5 раза, то есть температура
тоже увеличивается в 1,5 раза. Значит, суммарно температура увеличилась в 3 раза, и средняя кинетическая энергия увеличилась в
3 раза.
3)
Процесс 2-3 — изохорное нагревание. , следовательно,
Давление увеличивается в 1,5 раза, то есть температура
тоже увеличивается в 1,5 раза.
4)
Процесс 1-2 — изобарное расширение (). Объем увеличился в 2 раза, то есть температура тоже увеличилась в 2
раза.
5)
Уравнение состояния газа:
где — количество вещества,
— температура в Кельвинах,
— давление газа,
— объем, занимаемый газом,
—
универсальная газовая постоянная.
Температура максимальна там, где максимально произведение , поэтому из графика видно, что
,
.
Ошибка.
Попробуйте повторить позже
На рисунке показаны два процесса, проведённых с одним и тем же количеством газообразного неона ( – давление неона;
– его
объём).
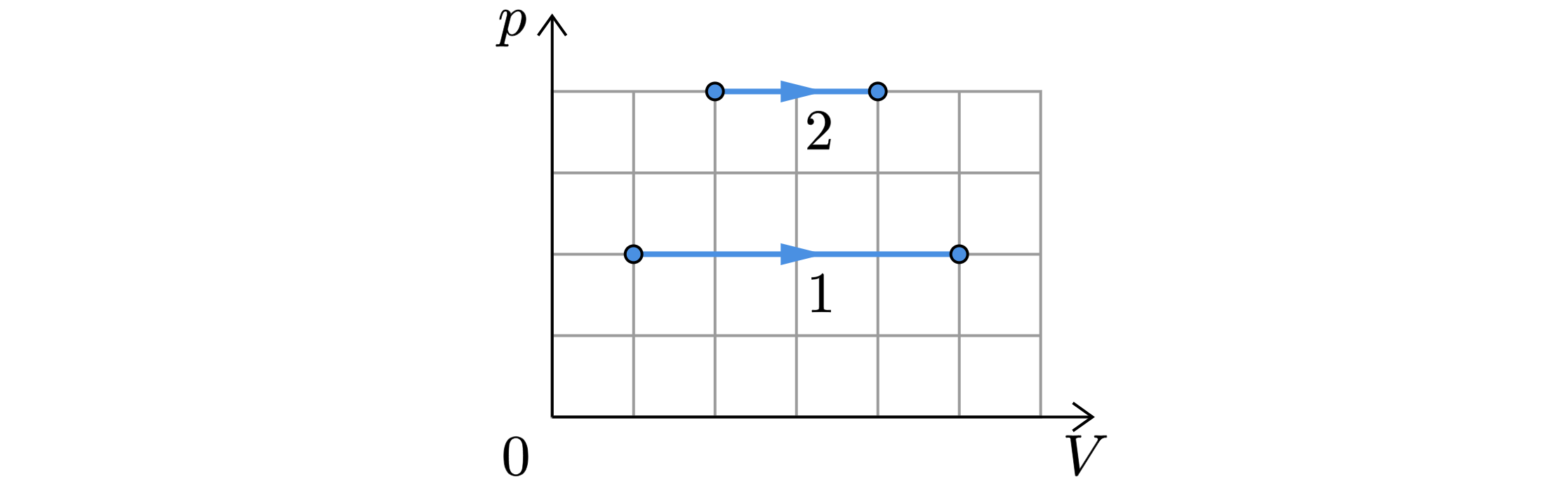
Из приведённого ниже списка выберите все верные утверждения, характеризующие процессы на рисунке.
1) В процессе 2 абсолютная температура неона изобарно увеличилась в 2 раза.
2) В процессе 1 плотность неона увеличилась в 5 раз.
3) Работа, совершённая неоном, в обоих процессах одинакова.
4) В процессе 1 объём неона изобарно увеличился в 4 раза.
5) В процессе 2 концентрация молекул неона уменьшилась в 2 раза.
1)
Из закона Менделеева-Клапейрона для постоянного количества газа:
где – температура,
– количество вещества,
– универсальная газовая постоянная.
Так как давление равно, а объём газа увеличился в 2 раза, то температура также увеличилась в 2 раза.
2)
Плотность равна:
где – масса газа.
Так как объем увеличился в 5 раз, то плотность уменьшилась в 5 раз.
3)
Работа газа в изобарном процессе:
Тогда для первого и второго процесса:
То есть работа газа в обоих процессах одинакова.
4)
Нет, объём увеличился в 5 раз.
5)
Концентрация:
где – количество молекул.
То есть при увеличении объёма в 2 раза концентрация уменьшилась в 2 раза.
Ошибка.
Попробуйте повторить позже
На рисунке представлены графики зависимости температуры двух тел одинаковой массы от сообщенного им количества теплоты
. Первоначально тела находились в твёрдом агрегатном состоянии.
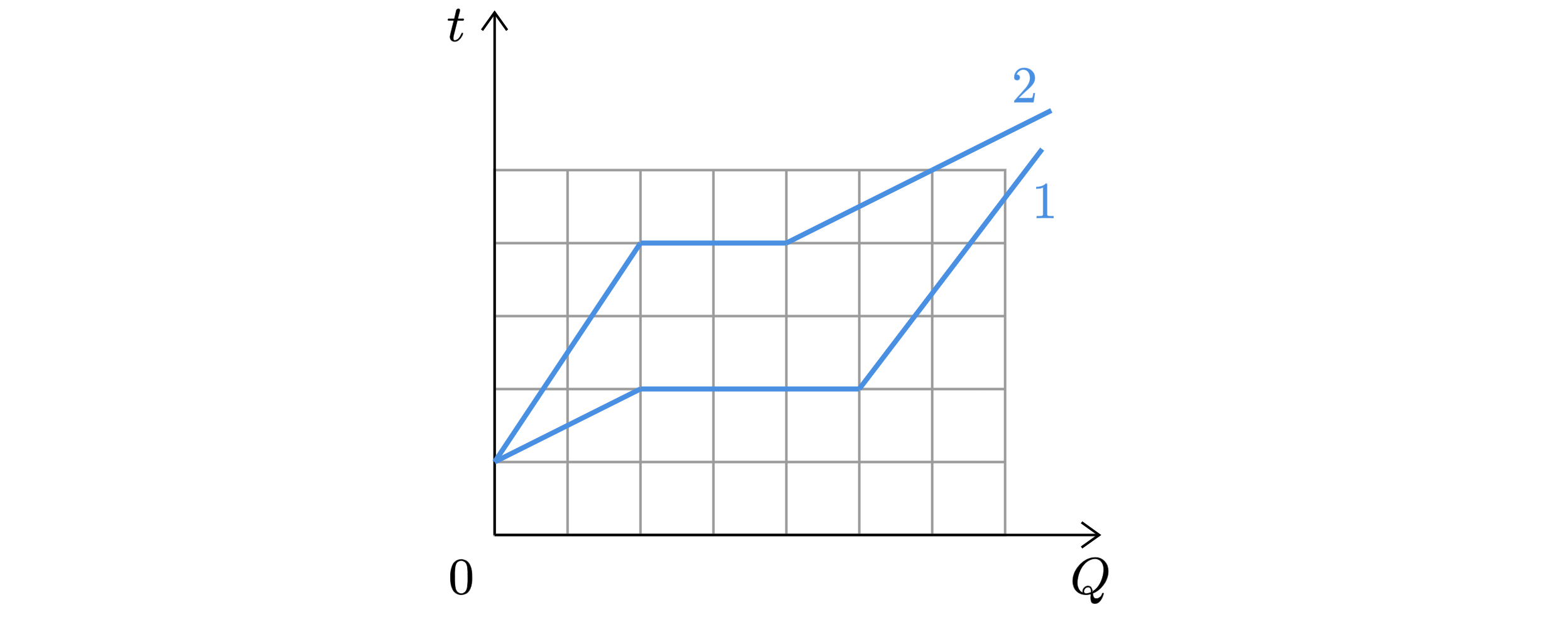
Используя данные графиков, выберите из предложенного перечня все верные утверждения.
1) Удельная теплота плавления первого тела больше удельной теплоты плавления второго тела.
2) Оба тела имеют одинаковую удельную теплоёмкость в жидком агрегатном состоянии.
3) Тела имеют одинаковую удельную теплоёмкость в твёрдом агрегатном состоянии.
4) Удельная теплоёмкость второго тела в твёрдом агрегатном состоянии в 3 раза больше, чем первого.
5) Температура плавления второго тела в 2 раза выше, чем температура плавления первого тела.
1)
Количество теплоты, необходимое для плавления:
где – удельная теплота плавления,
– масса тела.
То есть чем больше удельная теплота плавления, тем больше . Плавление – горизонтальный участок ломанной. Для тела 1
плавление составляет 3 клетки, для тела 2 – 2 клетки, то есть удельная теплота плавления у тела 1 больше, чем у тела 2.
2)
Для процесса нагрева справедлива формула:
где — удельная теплоемкость вещества,
— масса тела,
— изменение температуры.
То есть
Для того, чтобы теплоёмкость веществ была одинаковой, необходимо, чтобы наклоны прямых были одинаковы, а они разные,
значит, удельная теплоёмкость тел разные.
3) Для процесса нагрева справедлива формула:
где — удельная теплоемкость вещества,
— масса тела,
— изменение температуры.
То есть
Для того, чтобы теплоёмкость веществ была одинаковой, необходимо, чтобы наклоны прямых были одинаковы, а они разные,
значит, удельная теплоёмкость тел разные.
4)
Для процесса нагрева справедлива формула:
где — удельная теплоемкость вещества,
— масса тела,
— изменение температуры.
То есть
Тогда:
То есть удельная теплоёмкость второго тела в 3 раза меньше.
5)
Да, температура плавления – начало горизонтального участка ломанной, для первого тела температура плавления 2 клетки, а для
второго 4.
Ошибка.
Попробуйте повторить позже
На рисунке показан процесс изменения состояния одного моля одноатомного идеального газа ( – внутренняя энергия газа;
–
его давление). Используя данные графика, выберите из предложенного перечня все верные утверждения и укажите их
номера.
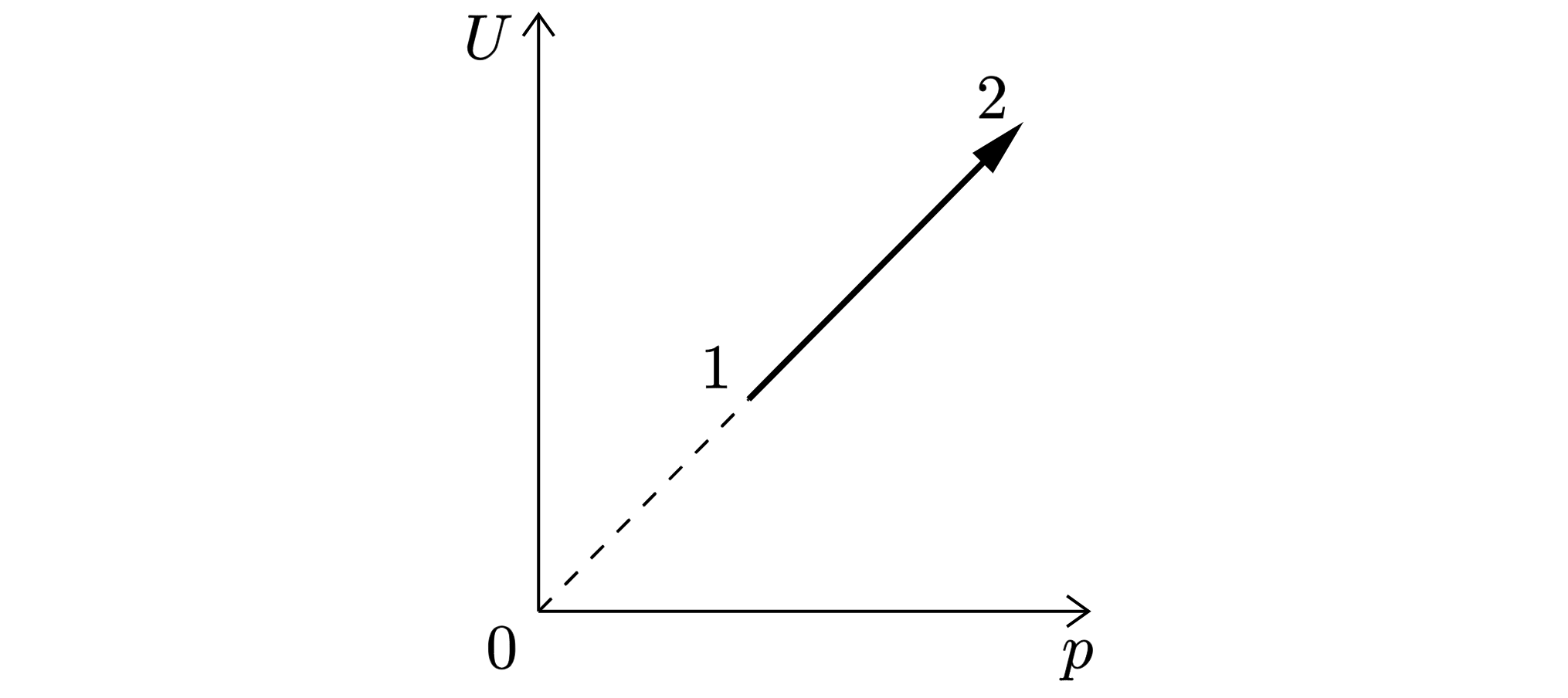
1) Концентрация молекул газа в ходе процесса уменьшается.
2) Объём газа в этом процессе остаётся неизменным.
3) Плотность газа в этом процессе увеличивается.
4) В ходе процесса газ расширяется.
5) Температура газа в ходе процесса повышается.
1)
, значит,
Запишем уравнение Менделеева-Клапейрона:
где — давление газа,
— объём,
— количество вещества,
— универсальная газовая постоянная,
— абсолютная
температура.
Отсюда
То есть объём постоянен. Так как объем и масса газа остается неизменными, то концентрация не меняется.
2)
Да, см. пункт 1
3)
Плотность равна:
где – масса газа.
По условию масса газа постоянна, а из пункта 1 объём газа постоянен, значит, плотность не изменяется.
4)
Нет см. пункт 1
5)
Да, см. пункт 1.
Ошибка.
Попробуйте повторить позже
В понедельник и вторник температура воздуха была одинаковой. Парциальное давление водяного пара в атмосфере в понедельник было меньше, чем во вторник. Из приведенного ниже списка выберите все правильные утверждения и укажите их номера.
1) Плотность водяных паров, содержащихся в воздухе, в понедельник была меньше, чем во вторник.
2) Относительная влажность воздуха в понедельник была меньше, чем во вторник.
3) Концентрация молекул водяного пара в воздухе в понедельник и вторник была одинаковой.
4) Давление насыщенных водяных паров в понедельник было больше, чем во вторник.
5) Масса водяных паров, содержащихся в 1 м воздуха, в понедельник была больше, чем во вторник.
1)
По уравнению Менделеева-Клапейрона:
где – давление,
– объём,
– масса водяных паров,
– молярная масса,
– температура.
Тогда плотность водяных паров
так как температуры одинаковы, то различия между плотностями обуславливается только различием давлений. Так как в понедельник давление меньше, то и плотность водяных паров в понедельник меньше.
2)
Относительная влажность воздуха определяется как:
где – парциальное давление водяного пара;
– давление насыщенного пара (табличная величина, зависящая только от
температуры).
Так как температуры одинаковы, а парциальное давление в понедельник меньше, чем во вторник, то и относительная влажность в понедельник меньше, чем во вторник.
3)
Давление водяного пара равно:
где – концентрация молекул,
– температура.
Так как по условию давление в понедельник было меньше, чем во вторник, то и концентрация молекул в понедельник была меньше.
4)
Нет, эта величина зависит от температуры, а температуры в понедельник и вторник были одинаковы.
5)
По уравнению Менделеева-Клапейрона:
где – давление,
– объём,
– масса водяных паров,
– молярная масса,
– температура.
Тогда
Так как давление в понедельник меньше, чем давление во вторник, то и масса водяных паров в понедельник меньше.
Ошибка.
Попробуйте повторить позже
При изучении явления теплообмена герметичный теплоизолированный сосуд с одноатомным идеальным
газом разделили неподвижной перегородкой, способной проводить тепло, на две одинаковые части (см.
рисунок). После этого газ в разных частях сосуда нагрели до разных температур. Температура газа в
части А равна 303 К, а в части Б равна . Количество газа одинаково в обеих частях
сосуда. Считая, что теплоёмкость сосуда пренебрежимо мала, выберите все утверждения,
которые верно отражают изменения, происходящие с газом в дальнейшем после окончания
нагревания.
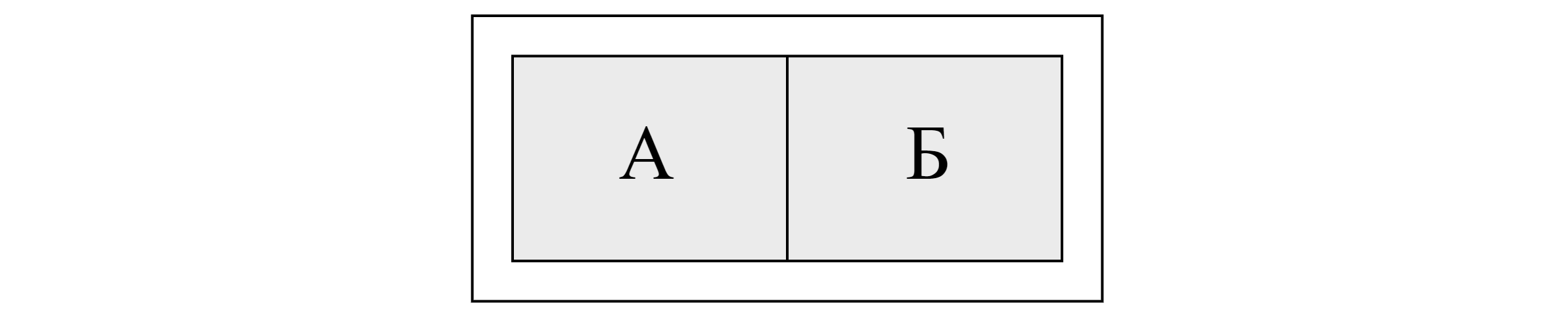
1) При теплообмене газ в части Б отдавал положительное количество теплоты, а газ в части А его получал.
2) Через достаточно большой промежуток времени температура газа в обеих частях сосуда стала одинаковой и равной 298 К.
3) Внутренняя энергия газа в части А не изменилась.
4) В результате теплообмена газа в сосуде А совершил работу.
5) Температура газа в части Б повысилась.
Найдём температуру части Б в Кельвинах К.
1)
Количество теплоты отдаёт газ с более высокой температурой, то есть газ в части А.
2)
Так как теплоёмкость сосуда пренебрежимо мала, то закон сохранения энергии газа запишется в
виде:
где – количество вещества,
и
– температуры в секциях А и Б соответственно,
–
конечная температура.
Тогда:
3)
Внутренняя энергия:
так как изменилась температура , то и изменилась и энергия.
4)
Перегородка неподвижна, объём не изменяется, значит, газ не совершает работу.
5)
Да, повысилась до 298 К.
Ошибка.
Попробуйте повторить позже
В жёстком герметичном сосуде объёмом при температуре 289 К длительное время находился
влажный воздух и 10 г воды. Сосуд медленно нагрели до температуры 298 К. Пользуясь таблицей
плотности насыщенных паров воды, выберите все верные утверждения о результатах этого
опыта
1) При температуре 23 влажность воздуха в сосуде была равна 48,5%.
2) В течение всего опыта в сосуде находилась вода в жидком состоянии.
3) Так как объём сосуда не изменялся, давление влажного воздуха увеличивалось пропорционально его
температуре.
4) В начальном состоянии при температуре 289 К пар в сосуде был насыщенный.
5) Парциальное давление сухого воздуха в сосуде не изменялось.
Демоверсия 2023
1)
Найдем, испарится ли вся вода в процессе. Пусть это не так, то масса водяного пара равна:
где – объём сосуда.
Тогда масса испаренной воды:
так как первоначально в сосуде было 10 г воды, то вся вода не испарилась, значит, пар остался
насыщенным и относительная влажность равна 100%
2)
Так как вся вода не испарилась в течении опыта, то пар все время является насыщенным.
3)
Пар в сосуде был насыщенным, следовательно, шел процесс испарения, поэтому давление влажного
воздуха не было прямо пропорционально его температуре.
4)
Так как вначале опыта в сосуда длительное время находилась вода и пар, то установилось равновесие и
пар стал насыщенным
5)
Давление сухого воздуха изохорически увеличивалось с ростом температуры по закону Шарля



